原创 重要突破!1型糖尿病治疗迎曙光!全球首例再生胰岛移植如何颠覆糖尿病治疗?
创始人
2026-03-18 21:48:43
0次
糖尿病治疗史上,1型糖尿病长期被视为“不可逆转的绝症”。患者因胰岛β细胞被免疫系统错误攻击,终身依赖胰岛素注射,承受并发症与低血糖风险。然而,2026年中国科研团队的一项里程碑式研究,为这一疾病带来了颠覆性变革——通过干细胞再生胰岛移植技术,首次实现胰岛功能重建与血糖自主调控,标志着糖尿病治疗从“对症控制”迈向“功能性治愈”。

一、技术突破:从“树根”到“树干”的范式革命
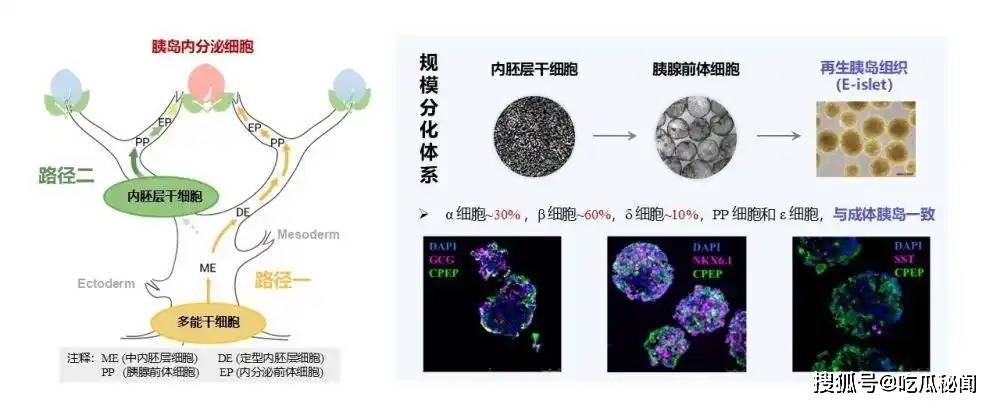
传统干细胞疗法依赖多能干细胞分化技术,需经历10余步复杂分化步骤,耗时长达5-6周,且存在未分化细胞残留导致成瘤的风险。而中国团队创新性地建立了“基于内胚层干细胞的技术体系”,直接从胰腺发育的“树干”阶段入手,实现三大突破:
- 定向分化精准化:内胚层干细胞仅朝胰腺、肝脏等目标细胞分化,避免了传统路径的“迷途”风险;
- 生产效率飞跃:分化步骤从10步精简至2步,生产周期缩短至2周,成本降低60%;
- 安全性跨越:内胚层干细胞体内无增殖能力,临床前实验显示安全性达100%,彻底消除成瘤隐患。
这一技术突破不仅攻克了供体短缺难题,更让大规模工业化生产再生胰岛成为可能。
二、临床验证:从个体治愈到普适性希望
研究团队完成了全球首例自体、中国首例异体及青少年病例的再生胰岛移植,覆盖不同年龄段与治疗路径:
- 病例一:30岁女性患者通过二次自体移植联合免疫抑制剂,胰岛功能完全恢复;
- 病例二:45岁暴发性1型糖尿病患者异体移植后36周彻底停用胰岛素,血糖稳定超2年;
- 病例三:15岁青少年患者术后低血糖事件消失,生活质量显著提升。
- 最长随访案例显示,患者实现临床治愈超26个月,C肽水平恢复正常,并发症进展有效阻断。这些成果验证了干细胞技术对不同群体的适用性,尤其为儿童患者提供了安全选项。
三、产业转化:从实验室到万亿市场的跨越
基于该技术的全球首个双批件药物“异体人再生胰岛注射液(E-islet01)”已获中美临床试验许可,预计2030年上市,覆盖中国近60万患者,市场规模达3000亿元。产业链协同创新同步推进:
- 上游:核心培养基与设备国产化率达80%,成本下降40%;
- 下游:与保险机构合作推出“治疗+疗效保障”套餐,降低支付压力;
- 国际合作:与诺和诺德等跨国药企联合研发低温存储与微创输注技术,加速全球化布局。
四、未来挑战与终极愿景
当前疗法仍需免疫抑制剂支持,团队正通过基因编辑技术开发“广义通用型”再生胰岛:
- 基因改造:敲除HLA基因使细胞“免疫隐身”;
- 安全开关:植入自杀基因应对异常增殖;
- 支付创新:探索“按疗效付费”模式,分阶段支付降低患者负担。
- 未来,糖尿病或将成为首个被干细胞技术攻克的慢性病,并为帕金森、癌症等疾病治疗提供范式。
相关内容
热门资讯
医生:冠心病最危险信号,不是心...
冠心病是中老年人群中最常见的心血管疾病之一,它的发病过程往往缓慢,初期可能毫无明显症状,这也是为什么...
28岁姑娘竟然查出胃癌晚期! ...
江苏28岁的小郭没有什么不良嗜好,仅仅是爱喝奶茶。2025年11月,她因巧克力囊肿在上海长海医院接受...
男人是真心还是敷衍?索要这1样...
“爱情是一场博弈,必须永远保持平等,才能长久依存。”——简·奥斯汀在《傲慢与偏见》中的这句话,道尽了...
糖尿病:到一定时间一定要打胰岛...
很多糖友都有这样的疑虑: “我现在吃着药血糖还行,但听说糖尿病时间长了都得打胰岛素,是真的吗?” “...
珠海心理咨询中心排行榜
理论界定:溯源与定义 认知失调理论(Cognitive Dissonance Theory)属社会心...
膳之幸:春分阴阳平,调和气血养...
“风雷送暖入中春,桃柳妆时日正新。”2026年3月20日春分携暖阳伴和风而来,昼夜均分,寒暑相平,阴...
重视减肥激素,减重不费力
正常的激素水平对人体功能有益,支持免疫系统功能和健康的睡眠-觉醒周期。然而,激素失衡,则会造成令人沮...
甘油三酯偏高不能吃橘子,医生劝...
血脂偏高的人平时饮食需要格外注意,尤其是甘油三酯水平高的人群,很多人可能没意识到水果虽然健康,但有些...
伊朗开展新一阶段“强力打击”,...
每经编辑|段炼 当地时间今天(3月17日)傍晚,伊朗伊斯兰革命卫队发布声明说,已实施“真实承诺4”...
熬夜、劳累最伤肝,乙肝人群这样...
肝脏是人体重要的代谢器官,对于乙肝人群来说,肝脏本身就处于相对脆弱的状态,日常的不良生活习惯,很容易...
狐大医 | 一次“摇树”引发胸...
出品 | 搜狐健康 作者 | 顺义妇儿医院儿科 肖菲 编辑 | 李冬梅 春季草长莺飞、阳光和煦,正是...
湿疹折磨夜不能寐,民间偏方不管...
你知道吗?在中国,每10个成年人里面就有至少3个人被湿疹困扰着。这个数字听起来是不是有点吓人?别以为...
南月敏:规范乙肝抗病毒治疗 预...
2026年3月18日是第26个“全国爱肝日”,今年的活动主题为“遏制肝硬化,远离肝癌”。为普及病毒性...
原创 重...
糖尿病治疗史上,1型糖尿病长期被视为“不可逆转的绝症”。患者因胰岛β细胞被免疫系统错误攻击,终身依赖...
过上不焦虑的生活,秘诀就是……
这几天我在翻看评论区留言时,发现很多朋友在倾诉自己的焦虑。有人说,看到别人生活中遭遇挫折,自己也开始...
自制水果沙拉,让你轻松“瘦”出...
想吃得健康又不耽误减脂?试试自制水果沙拉吧!它可是兼顾美味与健康的理想选择,既能满足你的口腹之欲,又...
原创 牛...
当我们谈论“健康饮食”时,牛肉似乎总是被贴上“高脂肪、高胆固醇”的标签。 很多人认为,牛肉是导致高...
这8种食物是糖尿病营养又有益的...
在平时生活中,对于糖尿病患者来说,除了需要定时注射胰岛素或者吃降糖药外,忌口也是十分关键的。我们常说...
西苑科普 | 睡好觉真能美容
很多人把美容寄托在护肤品、医美上,却忽略了天然的养颜之道——好好睡觉。《黄帝内经》的子午流注理论早已...
【汤医科普】春风暖,食宜安:春...
春季饮食 气温回暖,万物生发,但咱们的身体也进入了“换季疲劳期”。饮食不当、进补错误易导致感冒、过敏...
