卵巢癌免疫治疗的ATALANTE研究,阴性结果中看到希望
ATALANTE研究是一项关于阿替利珠单抗vs安慰剂 联合含铂化疗+贝伐珠单抗治疗铂敏感的复发性、非粘液性上皮性卵巢癌的III期研究,其试验设计如下图所示;主要终点是全人群以及PD-L1阳性人群(IC≥1%)的PFS(两个人群的α分别分配0.025),OS是次要终点。
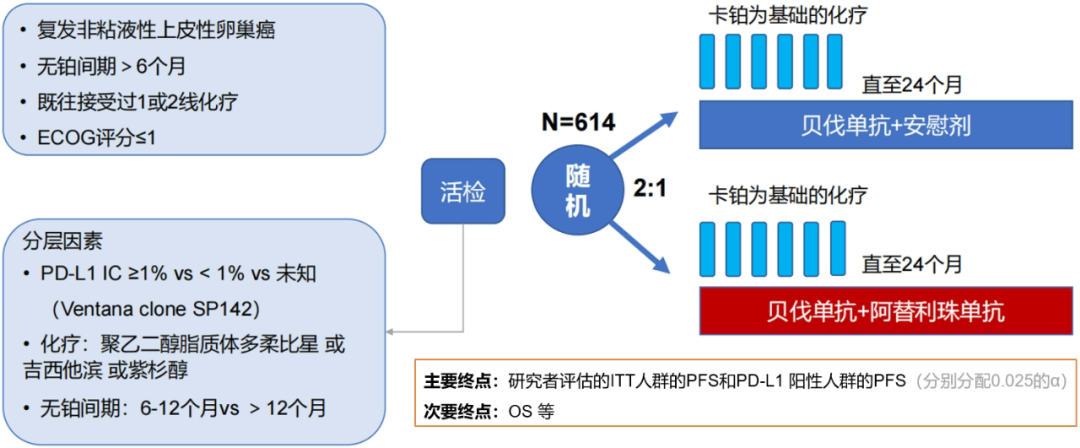
图1.试验设计
2022年ESMO年会上首次公布本试验的主要结果,全文于2023年8月发表于《Journal of Clinical Oncology》。此次报道的中位随访时间是36.6月。
在全人群中,试验组和对照组的mPFS分别是13.5月 vs 11.3月,试验组1年的PFS率(56% vs 46%)和2年的PFS(20% vs 12%)也高于对照组。从HR值来看,阿替利珠单抗可降低17%的疾病进展或死亡风险(HR=0.83),尤为重要的是,HR值的95%置信区间上限也小于1(0.69-0.99),显示出获益趋势。
但遗憾的是,经统计学检验,P值=0.041,高于预设的0.025,没有达到统计学阳性结果。
那么,我个人的理解是:全人群有获益,但获益的不多,不足以达到统计学上的差异。
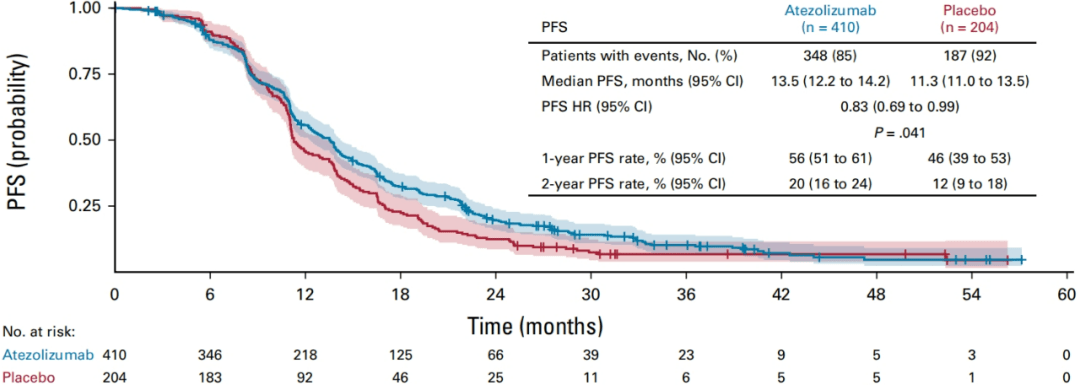
图2.全人群的PFS
在PD-L1阳性人群中(IC≥1%),观察到一样的情况:试验组的mPFS、1年PFS率和2年PFS率均高于对照组。
按道理来讲,PD-L1阳性人群对免疫治疗是更敏感的,应该获益更大;但本试验中PD-L1人群的HR值反而比全人群的高(HR=0.86),95%置信区间也跨1了(0.63-1.16)。如作者在去年ESMO上汇报更新结果时所讲的,本试验中PD-L1不能预测阿替利珠单抗的疗效。
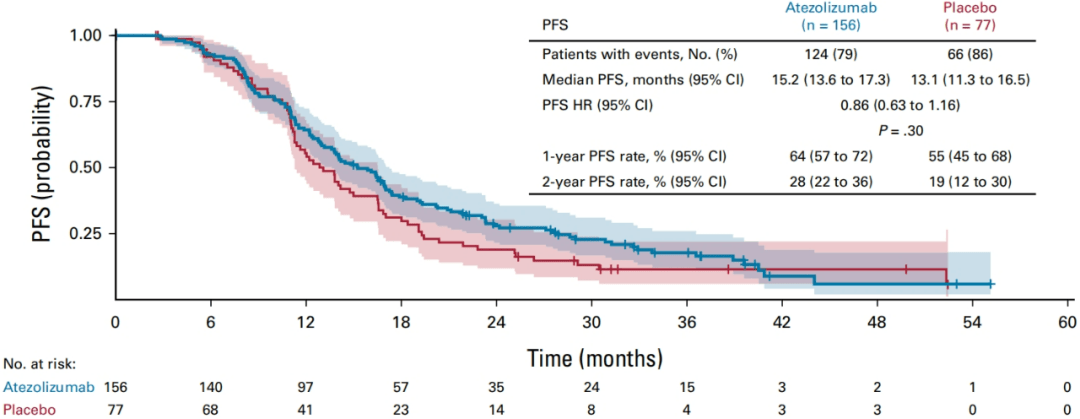
图3.PD-L1阳性人群的PFS
在全人群的PFS亚组分析中,有多个亚组的HR值95%置信区间始终小于1,意味着这些人群加用阿替利珠单抗后的疾病进展或死亡风险永远小于对照组。
其中,值得一提的是,与CD8/PD-L1双阳性的患者相比,阴性患者的获益反而更大(HR值更小,置信区间也小于1),这似乎与我们对免疫治疗的常规认识有所不同;当然,这也意味着CD8/PD-L1可能并不是十分可靠的预测疗效的标志物,从而鞭策我们继续探索更为精准的标志物。
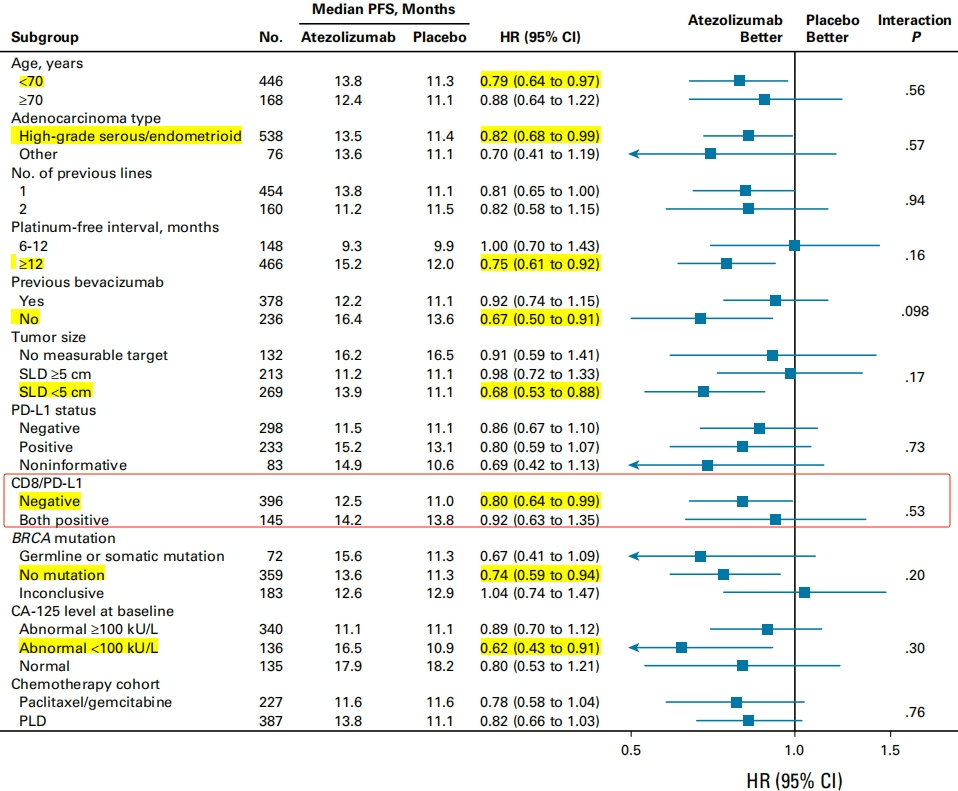
图4.全人群的PFS亚组分析
在全人群的OS方面,试验组的mOS比对照组提高近5个月(35.5月 vs 30.6月),死亡风险比值HR=0.81,此时的HR 95%置信区间还是跨1(0.65-1.01)。因为OS不是主要终点,所以没有统计检验,也就没有P值。
其实从生存曲线图来看,差不多从第16个月开始,两条曲线就始终保持分离,而且分离的很明显。
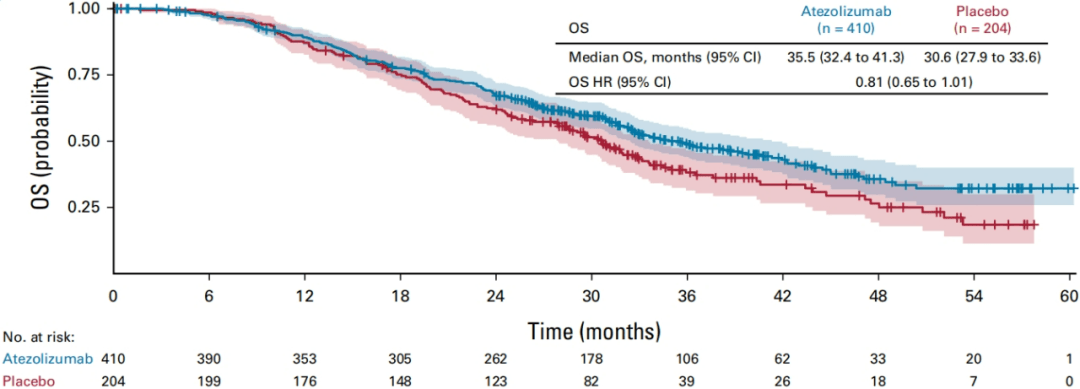
图5.全人群的OS
在去年的ESMO年会上,本试验公布了更新的结果,此时的中位随访时间是60.1月,较上次的随访时间延长了近2年。
经过更长时间的随访,PFS的结果与上次结果相似,依然是全人群获益的更大一些(HR始终小于1),PD-L1阳性人群获益小一些(HR值更大,置信区间跨1)
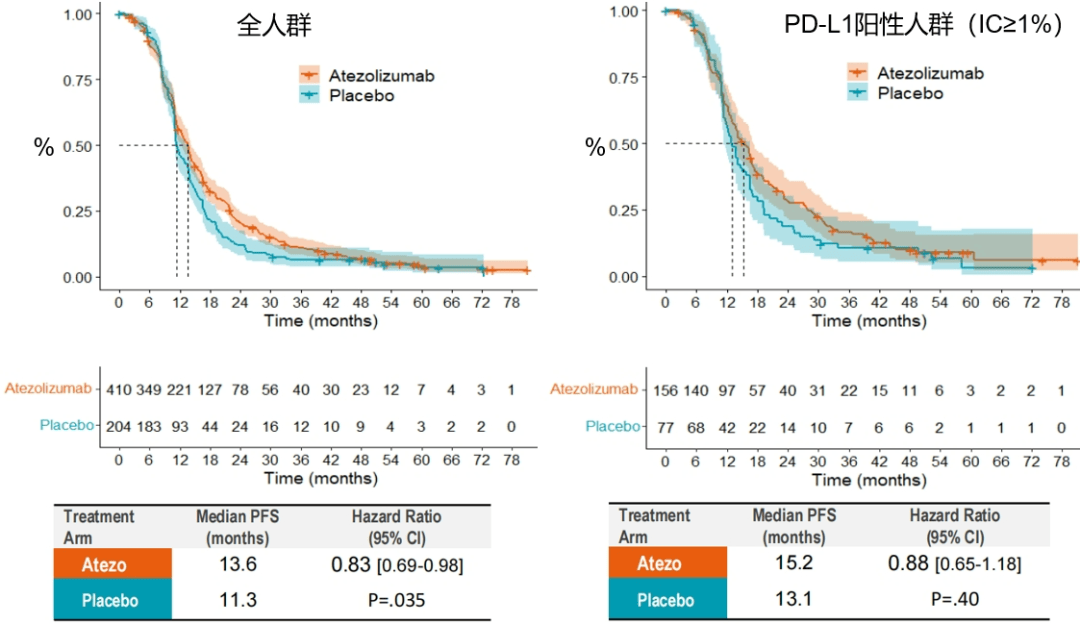
图6.更新的PFS结果
而令人兴奋的是:经过长达5年的随访,在全人群中,OS表现出明显的获益趋势。
mOS与上次结果相似,试验组mOS延长近5个月(35.75月 vs 30.62月)。
尤为关键的是:5年存活率从17%提高至27%,整整提高了10个点。试验组5年存活率的95%置信区间(23%~32%)的下限居然和对照组(12%~23%)的上限相持平;简单粗暴的理解:你(对照组)最高的5年存活率也只是和我(试验组)最差的5年存活率持平。
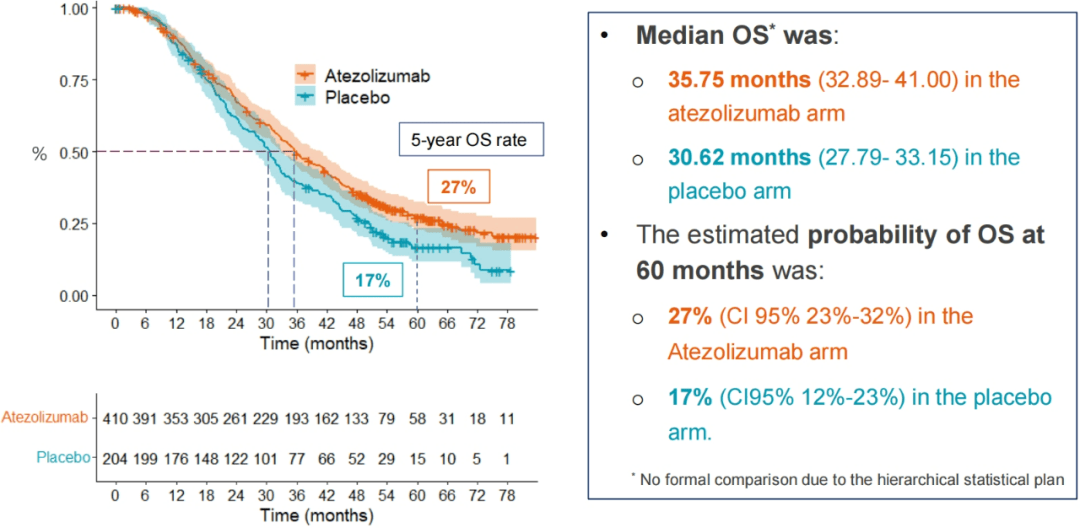
图7.更新的全人群OS
尽管在口头汇报的PPT里没有显示,但是在作者提交的ESMO摘要中显示:与上次的结果相比,全人群的死亡风险进一步降低(HR值从上次的0.81降到此次的0.79),HR值的95%置信区间始终小于1(0.65-0.96),这意味着对于加用阿替利珠单抗后的死亡风险始终比对照组要小。
唯一遗憾的是,因为OS不是主要终点,所以没有进行统计检验,也就无法判断这样的OS提高是否具有统计学差异。但是抛开统计,回归到临床,对于复发的卵巢癌患者,其5年的存活率可以提高10个点,这已经是一个巨大的飞跃,具有十分重要的临床意义!
结论:尽管主要终点(全人群和PD-L1阳性人群的PFS)没有达到统计学显著性;但是全人群PFS和OS的风险比值都小于1,提示加用阿替利珠单抗可降低疾病进展或死亡的风险;尤其是5年存活率可提高10个点。这些都十分具有临床意义!
延伸:
曾不止一位妇瘤的老师和我说:卵巢癌并不是完全对免疫治疗无效,只是我们还没有找到那些对免疫治疗有效的人群。
今天我依然坚定地相信这句话。
这也让我想起了阿替利珠单抗在卵巢癌的另一项III期研究:GOG-3015试验;关于阿替利珠单抗联合化疗+贝伐珠单抗一线治疗晚期卵巢癌。
我在之前曾详细分享过这项研究的内容,详情链接:
简而言之:把PD-L1 IC的界值从1%提高到5%,在IC≥5%的人群中观察到PFS和OS更加获益的趋势。同时,使用TC来评价PD-L1,在TC≥1%的人群中也看到更加明显的获益趋势。
也就是,同样是使用PD-L1作为标志物,不同的界值,或者不同的评价标准,得出的结果也不一样。这进一步提示PD-L1的不可靠性;也说明确实有那么一部分卵巢癌患者对免疫治疗敏感。
这也提示我们,在卵巢癌的免疫治疗中,寻找生物标志物的重要性。任重而道远!
值得关注的是:。对于铂耐药复发性卵巢癌,与化疗±贝伐珠单抗相比,加用帕博利珠单抗后显著提高了PD-L1阳性人群和全人群的PFS;尤为关键的是,PD-L1阳性人群的OS也得到显著改善!具体的研究数据预计会在今年10月份的ESMO年会上公布。
总之,这些研究都提示我们 卵巢癌并非对免疫治疗完全不敏感。
