宫颈切除术与消融术对生育影响的医学解析
宫颈癌前病变(如宫颈上皮内瘤变CIN2/3、高度鳞状上皮内病变HSIL)的临床处理中,宫颈切除术与消融术是常用治疗手段。然而,这类手术对生育功能的潜在影响一直是临床关注的重点。本文基于UpToDate最新医学证据,系统阐述两种术式对生育的影响机制、风险特征及管理策略。

治疗技术的生物学差异
01
宫颈切除术包括冷刀锥切术、环形电切术(LEEP/LLETZ)和激光锥切术,通过切除含病变的宫颈组织送病理检查,切除深度可达1-2cm,组织重量与体积直接影响术后风险。消融术则采用冷冻、激光、冷凝等技术破坏病变组织,保留原位组织且无需组织学确诊,对宫颈解剖结构的损伤显著小于切除术。这种结构性差异构成了两者生育影响差异的病理基础。
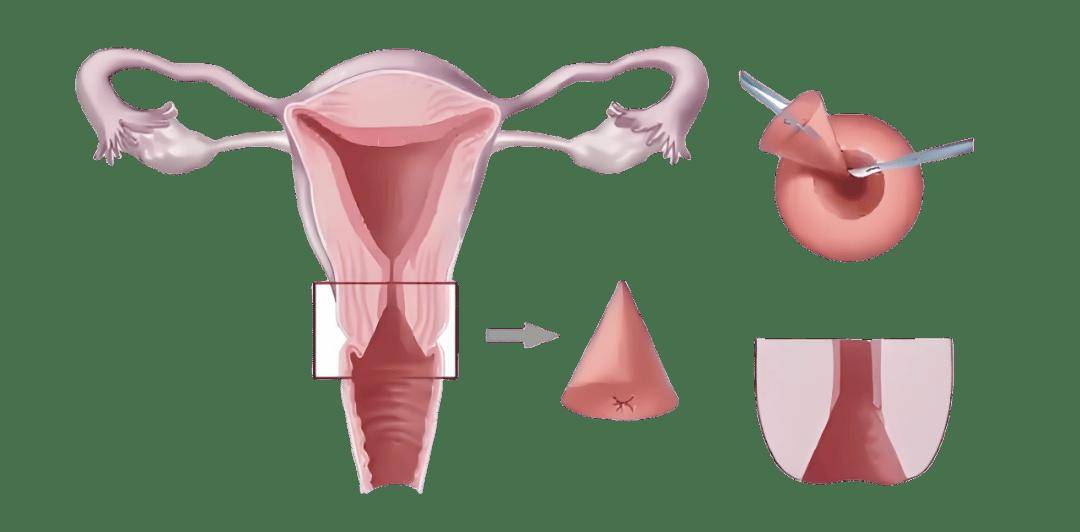
生育影响的病理生理学机制
02
手术对宫颈基质和腺体的破坏可引发多重生育风险。基质损伤会导致瘢痕形成,引发宫颈狭窄;同时降低宫颈拉伸强度,影响妊娠中晚期的宫颈机能。腺体破坏则减少宫颈黏液分泌及抗菌物质生成,破坏生殖道防御屏障,增加宫腔感染风险。研究显示,消融术因保留更多宫颈组织完整性,其不良产科结局发生率显著低于切除术。
妊娠前手术的生育风险谱
03
宫颈解剖结构异常
切除术后宫颈狭窄发生率可达8%,危险因素包括切除深度≥1-2cm及绝经后状态,可导致月经流出受阻、器械操作困难及精子迁移障碍。消融术相关狭窄率则≤1%,临床影响显著降低。
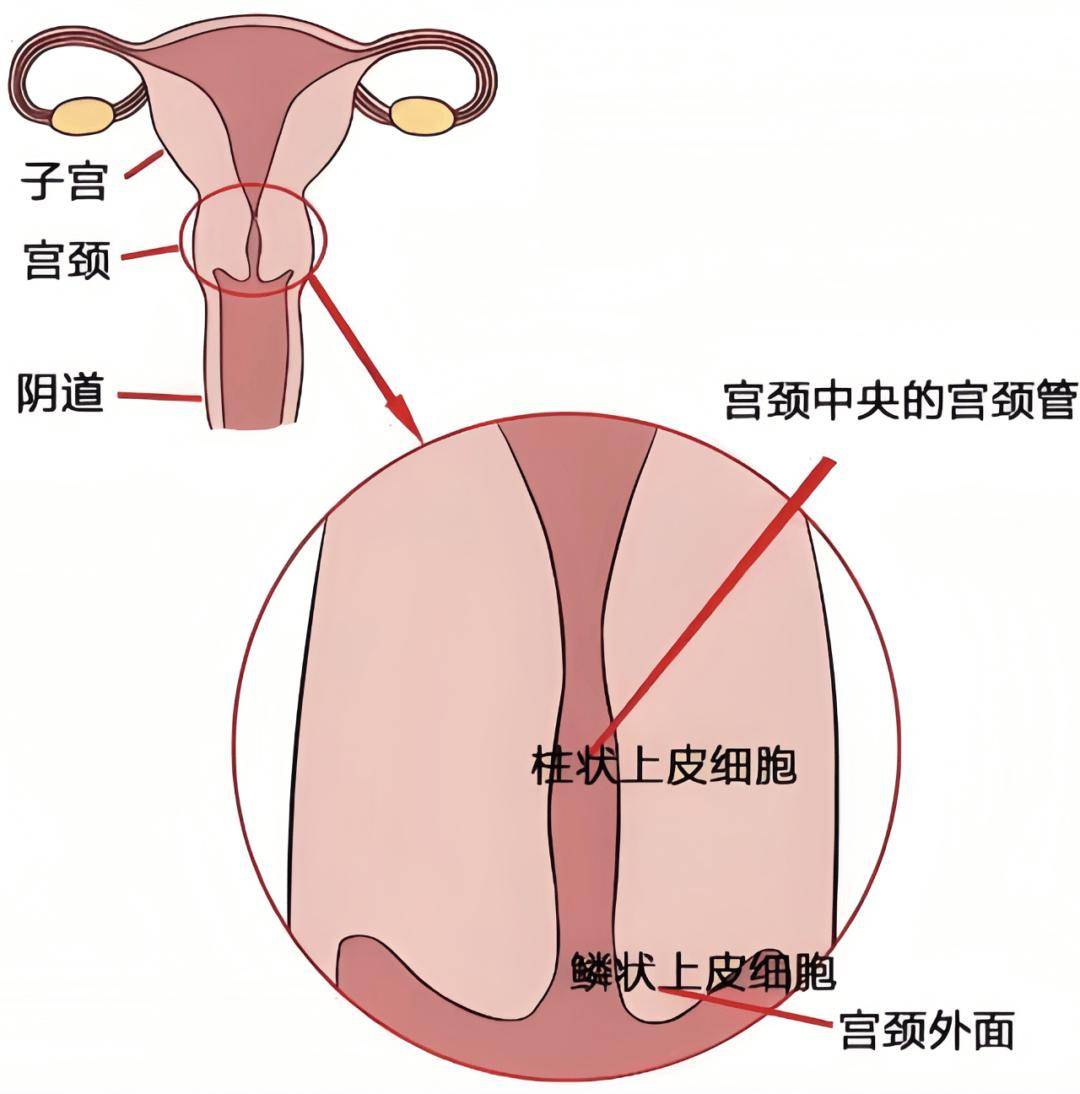
中期妊娠稳定性失衡
Meta分析显示,CIN治疗史与中期妊娠丢失风险升高相关(治疗组1.6% vs 未治疗组0.4%,RR 2.60),尤以LEEP(HR 3.0)和激光锥切术(HR 2.3)风险显著,且风险随切除组织量增加呈剂量依赖性。值得注意的是,此类手术不影响受孕率及早期妊娠丢失风险。
早产风险层级化分布
CIN治疗后早产风险呈多维度关联:
- 总体早产率:治疗组9.5% vs 未治疗组5.4%(RR 1.75),其中<32周早产风险达2.25倍
- 术式相关性:切除术早产率(11.2%)显著高于消融术(7.7%),冷刀锥切术风险最高(RR 2.70)
- 切除深度效应:切除深度>20mm时早产率达10.2%,呈线性递增趋势
围生育期管理的循证建议
04
受孕时机优化
推荐术后等待至少3个月再尝试受孕,以确保宫颈组织充分愈合。但需个体化评估:对高龄(接近40岁)患者,需权衡等待对生育力的潜在影响,避免过度延迟。
孕期监测体系构建
1. 超声监测方案:切除术后患者于孕16-20周行基线宫颈长度测量,随后每2周复测至孕28周;消融术患者按常规人群监测。
2. 干预阈值标准:孕24周前宫颈长度≤25mm时每周监测,≤20mm讨论环扎术,≤15mm推荐环扎术;宫颈长度>15mm者可经阴道补充孕激素。
分娩管理原则
分娩方式遵循标准产科指征,手术史不影响剖宫产决策阈值。需注意持续性宫颈狭窄可能导致难产,必要时需行剖宫产终止妊娠。

临床决策的风险效益平衡
05
宫颈癌前病变治疗的术式选择,本质是肿瘤防控与生育保护的权衡。切除术虽能提供明确的组织学诊断,但伴随更高的宫颈狭窄(8% vs 1%)、中期妊娠丢失(RR 2.6)及早产(RR 1.75)风险。消融术虽治疗失败率略高,但对生育功能影响显著更小。临床实践中,需结合病变级别、患者生育意愿及术式风险特征,制定个体化治疗方案。
对于有生育需求的患者,术后规范随访、孕期宫颈机能监测及适时干预,可显著改善妊娠结局。医学证据表明,通过科学管理,多数接受宫颈手术的女性仍可实现安全妊娠,体现了肿瘤防治与生育保护的现代医学平衡艺术。
有任何健康问题可以扫码联系小助理↓
别忘了
