[以药找靶] LiP-MS技术揭秘天然产物血根碱抑制口腔鳞状细胞癌进展
导读
天然产物结构多样、具有多靶点调节的生物活性,是新药发现的重要来源。明确天然产物的作用靶点,可以将传统经验用药转化为机制驱动的精准医疗,为药物研发和转化医学提供关键突破口。

摘要
口腔鳞状细胞癌(OSCC)是头颈部常见的恶性肿瘤。寻找高效、低毒的天然药物并明确其直接作用靶点一直是研发难点。这篇Phytomedicine(中科院1区,IF≈8.0)2025年的研究完整呈现了一套经典的“以药找靶”研究范式,层层递进揭示了天然产物血根碱(Sanguinarine/Sang)通过抑制PKM2酶活抑制肿瘤进展的机制。
研究流程
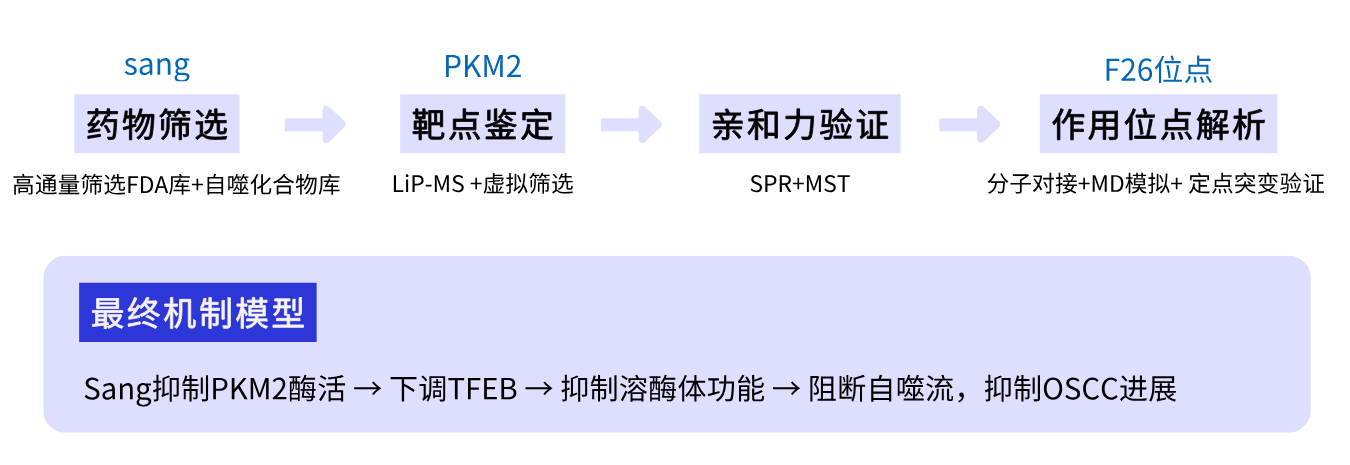
作用机制

研究内容
01. 高通量筛选
研究团队先用FDA批准药物库(2698个)+自噬化合物库(984个)进行高通量表型筛选(IncuCyte实时活细胞分析系统),在CAL27和SCC9两种OSCC细胞中同时筛选出仅2个强效化合物——多柔比星(阳性对照)和Sang。Sang抑制效果与多柔比星相当,但副作用更小,成为天然抗OSCC的优选候选。
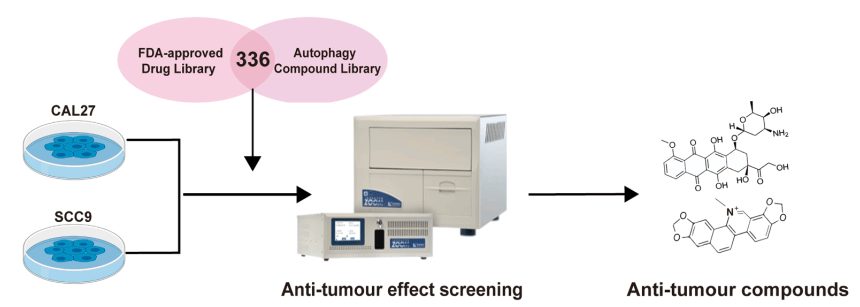
02. 以药找靶:LiP-MS“全扫描”捕获PKM2靶点+虚拟筛选辅助
Sang具有显著的抗癌活性,但在OSCC中的具体靶点和分子机制尚不明确。为了阐明对应的分子机制,本研究采用Limited Proteolysis-Mass Spectrometry(LiP-MS)化学蛋白质组学技术: Sang与蛋白结合后会“保护”特定酶切位点,导致肽段丰度发生特征性变化。 三浓度Sang处理CAL27细胞后,LiP-MS共鉴定出6个共同差异蛋白。

此外,结合虚拟筛选(Galaxy Sagittarius:结构+相似性双重预测),PKM2为唯一交集靶点。

03. 分子互作验证: SPR + MST定量亲和力
研究者进一步通过分子互作实验交叉验证了两者的直接结合:
· SPR(表面等离子共振): 动力学分析显示Sang与PKM2具有极强的亲和力7.3 μM,达到微摩尔级别。
· MST(微量热泳动):荧光标记PKM2与梯度Sang孵育,Kd = 2.6μM。

04. 结合位点解析:分子对接 + 分子动力学模拟 + 定点突变验证
分子对接预测得到了PKM2 与Sang 结合的3个潜在口袋。

此外,分子动力学模拟(100 ns,RMSD/RMSF/Rg/H-bond稳定性)锁定Site1最优。 MM-PBSA自由能计算显示F26残基贡献最大(ΔG最高),暗示其为结合的关键残基。

更进一步,构建PKM2 F26A突变体(KD&OE-WT vs KD&OE-F26A细胞系):
· 对接得分大幅下降,结合彻底消失
· Sang对PKM2酶活的抑制作用被完全逆转
· 自噬指标(MAP1LC3B-II、SQSTM1、TAX1BP1)、溶酶体功能(LAMP1/2、LysoSensor pH)、细胞增殖全部恢复
这些数据共同揭示F26就是Sang结合并抑制PKM2的核心位点。
05. 最终机制模型:PKM2/TFEB轴
结合一系列的后续功能验证实验,研究团队确认了机制:Sang结合PKM2 (F26位点为关键残基) 后,抑制了其酶活性。PKM2与转录因子TFEB存在相互作用,Sang通过靶向PKM2,下调TFEB表达。从而减少溶酶体相关膜蛋白、改变溶酶体pH等途径损害了溶酶体功能,阻断了自噬流,最终抑制OSCC的进展。
 Sang抑制口腔鳞状细胞癌进展的示意图模型:通过靶向 PKM2 抑制自噬流。
Sang抑制口腔鳞状细胞癌进展的示意图模型:通过靶向 PKM2 抑制自噬流。
总结与启示
本研究展示了现代质谱技术在天然产物靶点鉴定中的强大威力。
· 技术亮点: 放弃了传统的生物素标记法(可能干扰活性),直接利用 LiP-MS 在天然状态下筛选靶点,该技术还可提供结合区域序列信息。
· 转化意义: 证实了Sang不仅是一个多效能分子,更是一个精准的PKM2抑制剂,为口腔癌的药物开发提供了坚实的理论依据。
参考文献:
[1] Peng YC, He ZJ, Yin LC, et al. Sanguinarine suppresses oral squamous cell carcinoma progression by targeting the PKM2/TFEB aix to inhibit autophagic flux. Phytomedicine. 2025;136:156337. doi:10.1016/j.phymed.2024.156337
