子宫内膜异位症诊治指南(第三版)

子宫内膜异位症(内异症)是指子宫内膜组织(腺体和间质)在子宫腔被覆内膜及子宫以外的部位出现、生长、浸润,反复出血,继而引发疼痛、不孕及结节或包块等。内异症是生育年龄妇女的多发病、常见病。内异症病变广泛、形态多样、极具侵袭性和复发性,具有性激素依赖的特点。内异症的真正患病率尚无确切的数据。
01内异症的发病机制
内异症的发生与性激素、免疫、炎症、遗传等因素有关,但其发病机制尚不明确。以Sampson经血逆流种植为主导理论,逆流至盆腔的子宫内膜需经黏附、侵袭、血管性形成等过程得以种植、生长、发生病变;在位内膜的特质起决定作用,即“在位内膜决定论”;其他发病机制包括体腔上皮化生、血管及淋巴转移学说以及干细胞理论。最新的研究观点为,内异症与基因、表观遗传学、血管新生、神经新生、上皮间质转化、孕激素抵抗、异常增殖和凋亡、炎症等多种因素密切相关。
02内异症的临床诊断
内异症是妇科常见的慢性疾病之一,普遍存在诊断延迟的情况。诊断延迟则可导致病情加重,进一步影响疾病治疗及预后,增加复发风险,降低患者的生命质量。因此,早期诊断内异症尤为重要。临床诊断对于内异症的早期干预和治疗有非常重要的意义。
1. 内异症的临床表现为以下1种或多种:
(1)痛经,影响日常活动和生活。(2)慢性盆腔痛。(3)性交痛或性交后疼痛。(4)与月经周期相关的胃肠道症状,尤其是排便痛;以及与月经周期相关的泌尿系统症状,尤其是血尿或尿痛。(5)合并以上至少1种症状的不孕。具有以上1种或多种症状可以临床诊断内异症。
2. 其他症状:
侵犯特殊器官的内异症常伴有其他症状。肠道内异症常有消化道症状,如便频、便秘、便血、排便痛或肠痉挛,严重时可出现肠梗阻。膀胱内异症可出现尿频、尿急、尿痛甚至血尿。输尿管内异症常发病隐匿,多以输尿管扩张或肾积水就诊,甚至会出现肾萎缩、肾功能丧失。如果双侧输尿管及肾受累,可有高血压症状。肺及胸膜内异症可出现经期咯血、气胸。剖宫产术后腹壁切口、会阴切口内异症表现为瘢痕部位结节伴有与经期密切相关的疼痛。
3. 体征:
通过妇科检查(双合诊、三合诊)了解盆腔情况,内异症的典型体征为子宫后倾固定、附件可扪及活动度欠佳的囊性肿块,阴道后穹隆、直肠子宫陷凹、宫骶韧带痛性结节、阴道后穹隆紫蓝色结节。妇科检查的结果受医师的经验及技巧影响极大,但对诊断内异症有重要意义,尤其是深部浸润型内异症(deep infiltrating endometriosis,DIE)病灶多位于后盆腔,因此三合诊显得尤为必要,阴道后穹隆、阴道直肠隔痛性结节可考虑DIE(证据等级:Ⅲ级)。三合诊不适用于无性生活的患者,对于早期、比较表浅的病灶也无法作出诊断。
4. 影像学检查:
影像学检查的敏感性因内异症的病灶部位不同而有差异。对于卵巢子宫内膜异位囊肿和深部内异症的诊断,超声检查敏感。
5. 生物标志物:
迄今为止,外周血及子宫内膜的多种标志物,尚无一种能准确诊断内异症。 CA125水平检测对早期内异症的诊断意义不大。 CA125水平升高更多见于重度内异症、盆腔有明显炎症反应、合并子宫内膜异位囊肿破裂或子宫腺肌病者。
6. 其他特殊检查:
可疑膀胱内异症或肠道内异症,术前应行膀胱镜或肠镜、经肠道超声检查并行活检,以除外器官本身的病变特别是恶性肿瘤。
03内异症的药物治疗
内异症的长期管理应最大化发挥药物治疗的作用。内异症的治疗药物主要分为非甾体类抗炎药(NSAID)、孕激素类、复方口服避孕药(COC)、促性腺激素释放激素激动剂(GnRH-a)及中药五大类。因内异症无法治愈,药物治疗需有效并安全,持续使用到绝经或计划妊娠时;计划妊娠的患者完成生育后,应尽快继续恢复药物长期管理。药物治疗以长期坚持为目标,选择疗效好、耐受性好的药物。
1. NSAID:
(1)作用机制:①抑制前列腺素的合成;②抑制淋巴细胞活性和活化的T淋巴细胞的分化,减少对传入神经末梢的刺激;③直接作用于伤害性感受器,阻止致痛物质的形成和释放。但不能延缓内异症的进展。
(2)用法:推荐与孕激素或COC联用;根据需要应用,间隔不少于6 h。
(3)副作用:主要为胃肠道反应,偶有肝肾功能异常。长期应用要警惕胃溃疡的可能。
2. 孕激素类
作用机制:孕激素可引起子宫内膜蜕膜样改变,最终导致子宫内膜萎缩,同时,可负反馈抑制下丘脑-垂体-卵巢(HPO)轴。包括:地诺孕素(2 mg/d,口服),甲羟孕酮,注射用长效甲羟孕酮,左炔诺孕酮宫内缓释系统(LNG-IUS),地屈孕酮[10~20 mg,每月21 d(第5~25天)],孕三烯酮(2.5 mg,2~3次/周,共6个月)等。
副作用:主要是突破性出血、乳房胀痛、体重增加、消化道症状及肝功能异常。
新型孕激素地诺孕素(2 mg/d)有中枢和外周的双重作用机制,缓解内异症痛经的同时可以缩小卵巢子宫内膜异位囊肿,并且随用药时间的延长,缩小异位囊肿的效果更显著。由于其日剂量低,对肝肾功能及代谢影响小,耐受性好,长期应用1年以上的有效性和安全性证据充足,可作为内异症长期管理的首选药物。
3. COC:
(1)作用机制:抑制排卵;负反馈抑制HPO轴,形成体内低雌激素环境。
(2)用法:连续或周期用药。
(3)副作用:较少,偶有消化道症状或肝功能异常。40岁以上或有高危因素(如糖尿病、高血压、血栓史及吸烟)的患者,要警惕血栓的风险。
4. GnRH-a:
(1)作用机制:下调垂体功能,造成暂时性药物去势及体内低雌激素状态。也可在外周与GnRH-a受体结合,抑制在位和异位内膜细胞的活性。
(2)用法:依不同的制剂有皮下注射或肌内注射,每28天1次,共用3~6个月或更长时间。
(3)副作用:主要是低雌激素血症引起的围绝经期症状,如潮热、阴道干燥、性欲下降、失眠及抑郁等。长期应用则有骨质丢失的可能。
(4)GnRH-a+反向添加(add-back)方案:理论基础:“雌激素窗口剂量理论”学说,不同组织对雌激素的敏感性不一样,将体内雌激素的水平维持在不刺激异位内膜生长而又不引起围绝经期症状及骨质丢失的范围[雌二醇水平在146~183 pmol/L(即40~50 pg/ml)之间],则既不影响治疗效果,又可减轻副作用。
反向添加方案:①雌孕激素方案:雌孕激素连续联合用药。雌激素可以选择:戊酸雌二醇0.5~1.0 mg/d,或每天释放25~50 μg的雌二醇贴片,或雌二醇凝胶1.25 g/d经皮涂抹;孕激素多采用地屈孕酮5 mg/d或醋酸甲羟孕酮2~4 mg/d。也可采用复方制剂雌二醇屈螺酮片,1片/d。②连续应用替勃龙,推荐1.25~2.5 mg/d。反向添加的注意事项:①何时开始反向添加尚无定论。②应用反向添加可以延长GnRH-a使用时间。治疗剂量应个体化,有条件者应监测雌激素水平。
(5)GnRH-a与联合调节:3个月内的GnRH-a短期应用,只为缓解症状的需要,也可以采用植物药,如黑升麻异丙醇萃取物、升麻乙醇萃取物,每天2次,每次1片。
(6)GnRH-a与序贯治疗:GnRH-a在长期管理中还可以与其他药物序贯使用,不仅可以维持治疗,还能减轻后续药物治疗初期的副作用。例如,不规则出血是孕激素应用初期的常见问题,GnRH-a短期预处理可强效萎缩子宫内膜,可以减少孕激素治疗初期的不规则出血。证据显示,GnRH-a预处理可以降低LNG-IUS的脱落率,延长续用。
5. 中药:
中药可以有效缓解痛经症状。
04内异症相关疼痛的治疗
1. 治疗原则:
(1)未合并不孕及附件包块直径<4 cm者,首选药物治疗;(2)合并不孕或附件包块直径≥4 cm者考虑手术治疗;(3)药物治疗无效可考虑手术治疗。内异症相关疼痛的诊治流程见图1。
图1 内异症相关疼痛的诊治流程图
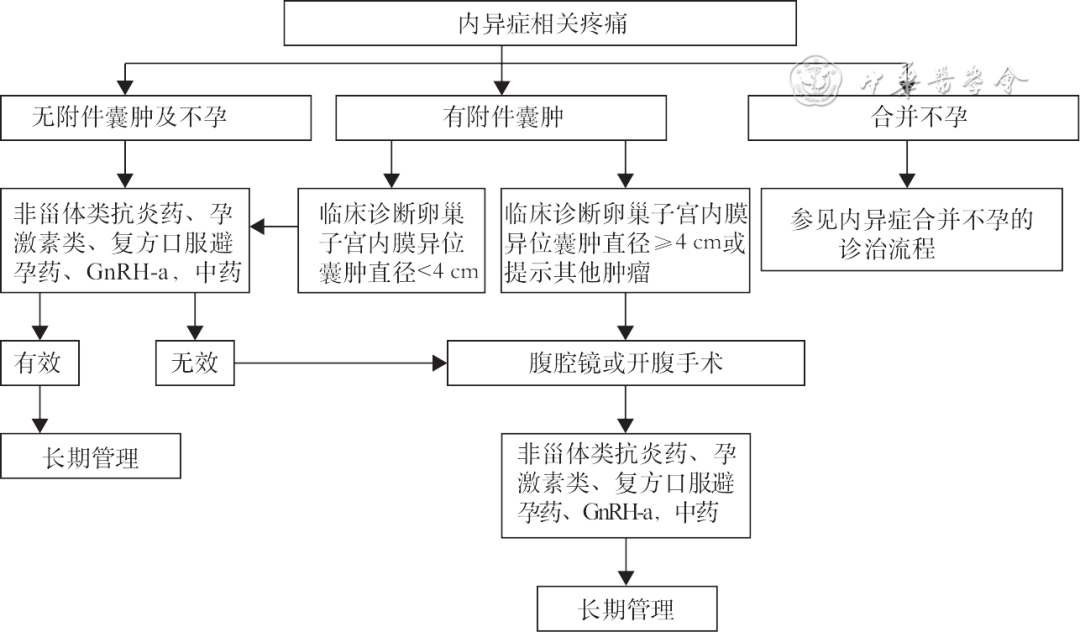
注:内异症表示子宫内膜异位症;GnRH-a表示促性腺激素释放激素激动剂
2. 药物治疗:
见前文“内异症的药物治疗”。
3. 手术治疗:
手术以腹腔镜手术为首选。应有仔细的术前评估和准备,良好的手术设备,合理的手术方式,熟练的手术技术,以及合适的术后处理方案。
手术方法包括:盆腔粘连松解术,内异症病灶切除术,卵巢囊肿剔除术,一侧附件切除术,子宫腺肌病病灶切除术,子宫全切除加双侧附件切除术,DIE(肠、膀胱、阴道、盆腔等)病灶切除术等。保守性手术后复发率较高,故手术后应辅助药物治疗并长期管理。
